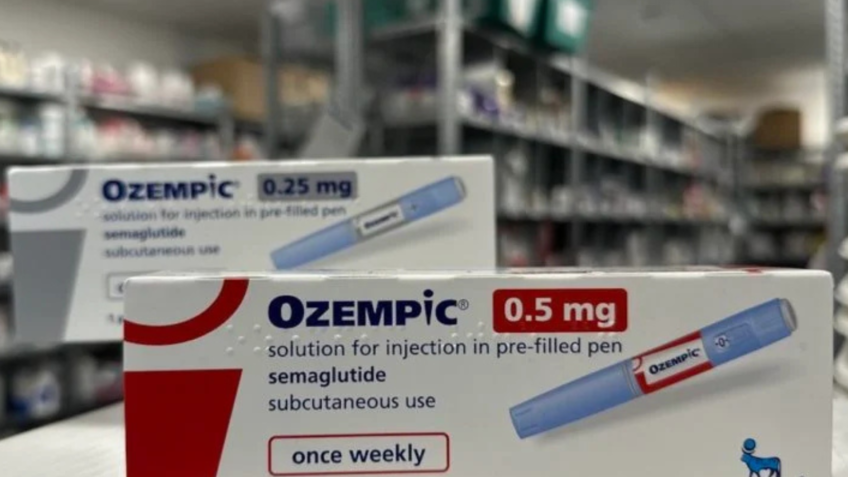
Recente decisão da Anvisa obriga retenção de receita para compra do medicamento; entidades pedem proibição de análogos
A Interfarma (Associação da Indústria Farmacêutica de Pesquisa) disse na 5ª feira (17.abr.2025) que a exigência da retenção de receita para a compra de medicamentos como Ozempic, Wegovy e Mounjaro “não enfrenta a causa raiz do problema”. A Anvisa (Agência Nacional de Vigilância Sanitária) decidiu na 4ª feira (16.abr) tornar obrigatória a retenção da prescrição na venda das canetas emagrecedoras.
Em nota, a entidade defendeu que o foco deveria estar no combate ao mercado irregular e na proibição integral da manipulação de análogos de GLP-1 –hormônio intestinal que ajuda a regular o apetite e os níveis de açúcar no sangue.
“Este mercado vem realizando a importação e manipulação em escala industrial de princípios ativos sem qualquer garantia de qualidade, segurança ou eficácia – muitas vezes promovidas com fins estéticos, por meio de campanhas publicitárias irregulares e direcionadas ao público leigo”, afirmou.
A preocupação é compartilhada pelo Sindusfarma (Sindicato da Indústria de Produtos Farmacêuticos), que também pediu à Anvisa que vete a manipulação de compostos da classe. Segundo as associações, farmácias estariam importando insumos sem controle de origem, qualidade ou eficácia.
A Interfarma destacou que essas farmácias não seguem as mesmas normas de Boas Práticas de Fabricação exigidas das indústrias registradas e que isso pode gerar riscos à saúde, como superdosagem, subdosagem, contaminação e instabilidade dos produtos.
Eis a íntegra da nota da Interfarma:
“A Interfarma (Associação da Indústria Farmacêutica de Pesquisa) alerta que a decisão da Anvisa de estabelecer a obrigatoriedade de retenção de receita para medicamentos análogos de GLP-1, usados no tratamento de diabetes tipo 2 e obesidade, não enfrenta a causa raiz do problema.
“A retenção de receitas, por si só, não resolverá o crescente mercado paralelo de manipulação dos análogos de GLP-1. Este mercado vem realizando a importação e manipulação em escala industrial de princípios ativos sem qualquer garantia de qualidade, segurança ou eficácia – muitas vezes promovidas com fins estéticos, por meio de campanhas publicitárias irregulares e direcionadas ao público leigo. Não sendo provenientes dos fabricantes dos medicamentos de referência e detentores das respectivas patentes, esses IFAs não têm procedência reconhecida e homologada, colocando a saúde da população em risco.
“Levantamentos recentes indicam um volume expressivo de insumos importados para esse fim, suficiente para fabricar de forma irregular 4 milhões de produtos com semaglutida e 2 milhões com tirzepatida de 5 mg, o que reforça a urgência de ações mais contundentes.
“Ainda que a RDC nº 67/200 preveja a manipulação de medicações de acordo com prescrições individualizadas diferentes daquelas aprovadas comercialmente, a manipulação em escala industrial contraria a legislação e alimenta o mercado irregular, inclusive sem prescrição. Os produtos manipulados não passam por avaliação da Anvisa, contrariando normas como a RDC nº 67/2007, e representam sérios riscos à saúde, incluindo subdosagem, superdosagem, contaminação e falta de estabilidade, comprometendo a eficácia e a segurança. O voto do diretor-presidente substituto Rômison Mota enfatiza que a manipulação não serve para produção em larga escala, até porque se assim fosse, as regras sanitárias deveriam ser as mesmas.
“Por isso, a Interfarma reforça que o foco deve ser o combate efetivo ao mercado irregular de medicamentos, com fortalecimento da fiscalização, controle de fronteiras, garantia da rastreabilidade de insumos farmacêuticos ativos e proibição integral da manipulação de análogos de GLP-1 – como já ocorre na Austrália e África do Sul, e com sérias restrições nos Estados Unidos. Apenas com uma atuação coordenada e rigorosa será possível proteger, de fato, a saúde da população.”